顯微鏡影像處理中的人工智能
人工智能正在以精確分割、降噪、超解析度和自動影像擷取等強大功能,徹底改變顯微鏡影像處理。本文重點介紹科學研究中重要的人工智能工具與新興趨勢。
人工智能技術正在革新顯微鏡領域,透過優化影像擷取與自動化分析。在現代智慧顯微鏡中,人工智能模組能即時調整成像參數(如焦距、照明),以減少光漂白並提升訊號品質。同時,深度學習演算法能從複雜的影像資料中篩選出隱藏的生物學洞見,甚至將影像與其他資料(如基因組學)連結。
人工智能方法:機器學習與深度學習
人工智能方法涵蓋經典的機器學習(ML)與現代的深度學習(DL),兩者各有優勢與限制:
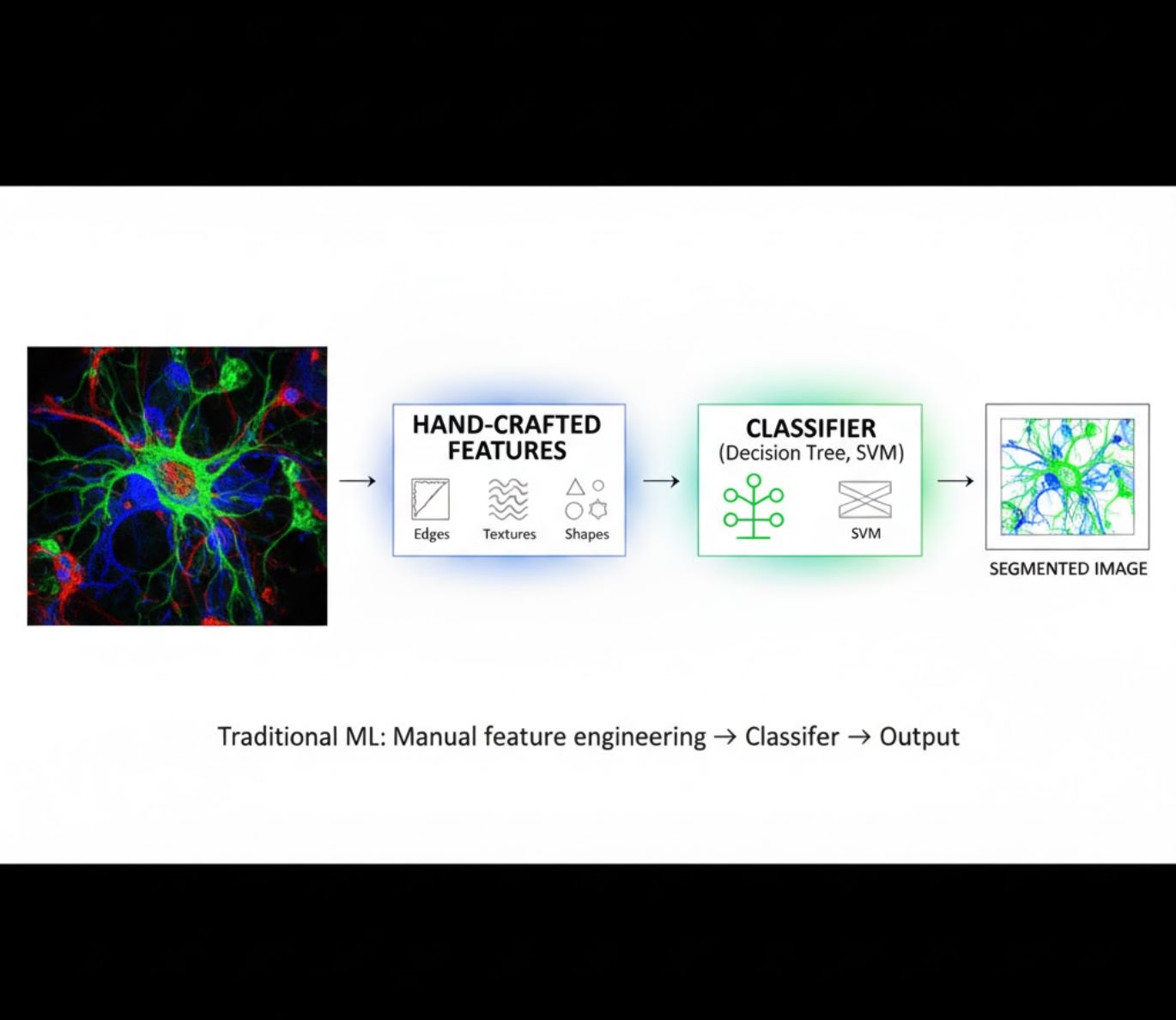
手工設計特徵
- 研究者手動設計影像特徵(邊緣、紋理、形狀)
- 將特徵輸入分類器(決策樹、支持向量機)
- 訓練速度快
- 對複雜或噪聲影像表現較差
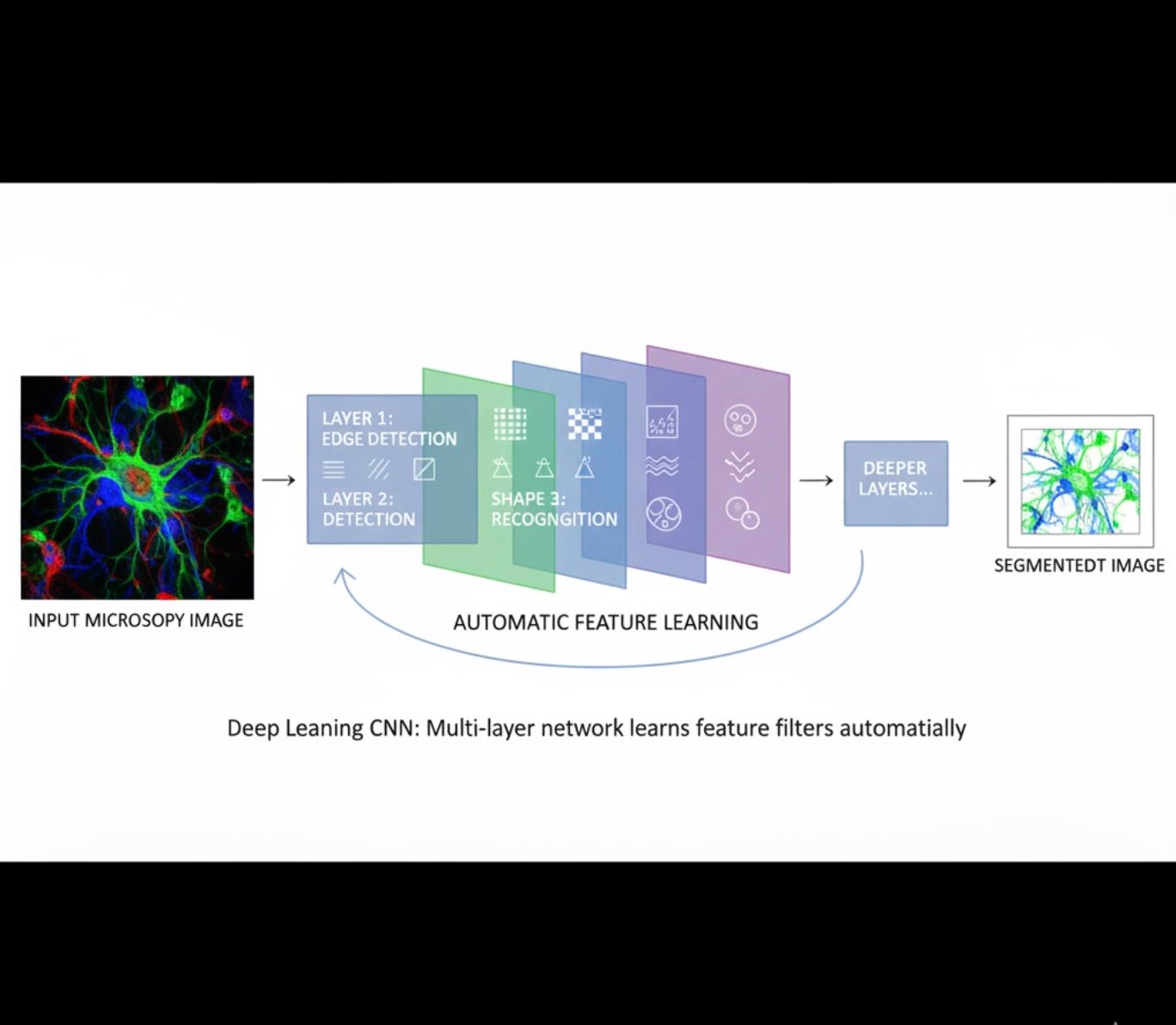
自動特徵學習
- 多層神經網路(CNN)自動學習特徵
- 從原始像素端到端學習
- 對變異更具魯棒性
- 可靠捕捉複雜紋理與結構
CNN運作原理:卷積神經網路對顯微鏡影像施加連續濾波器,早期層學習偵測簡單模式(邊緣),深層則捕捉複雜結構(細胞形狀、紋理)。這種階層式學習使深度學習在強度變化大時仍具高度穩健性。
視覺比較:機器學習與深度學習流程
顯微鏡中人工智能的主要應用
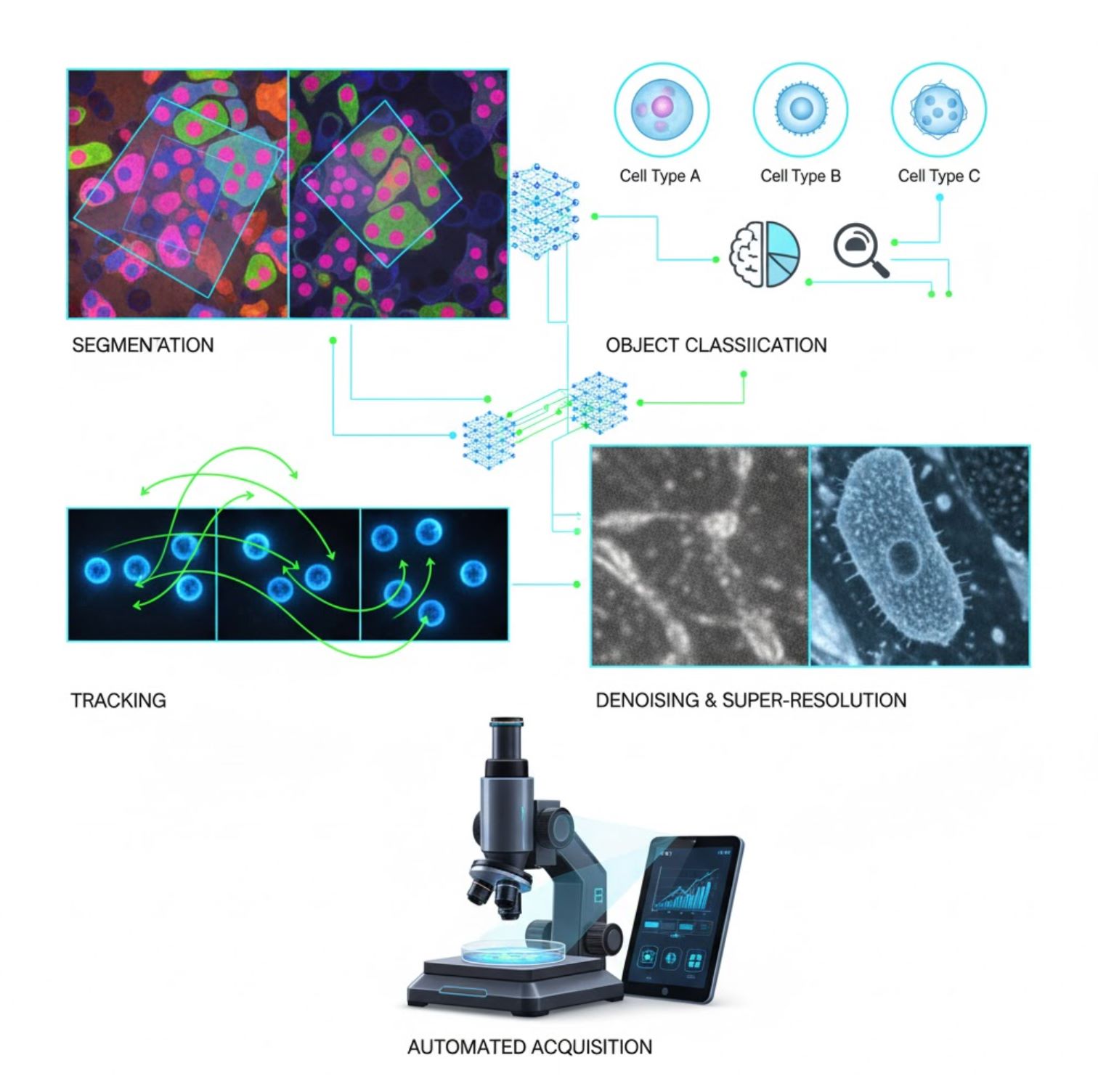
人工智能已嵌入顯微鏡工作流程中的多項影像處理任務:
分割
將影像劃分為不同區域(如識別每個細胞或細胞核)。深度網路如U-Net在此任務表現優異。
- 語義分割:每像素分類標籤
- 實例分割:分離個別物件
- 在擁擠或暗淡影像中具高準確度
- 視覺基礎模型(如μSAM)現已適用於顯微鏡
物件分類
分割後,人工智能能高精度分類每個物件。
- 細胞類型識別
- 有絲分裂階段判定
- 病理指標檢測
- 辨識難以手動量化的微妙表型
追蹤
在時間序列顯微鏡中,人工智能能以前所未有的準確度追蹤細胞或粒子。
- 深度學習大幅提升追蹤準確性
- 實現移動細胞的可靠分析
- 捕捉動態生物過程
降噪與超解析度
人工智能模型透過去除噪聲與模糊來提升影像品質。
- 物理知識導向的深度模型學習顯微鏡光學
- 重建更銳利、無人工痕跡的影像
- 相較傳統方法,解析度更高且減少偽影
自動擷取
人工智能即時引導顯微鏡操作。
- 分析即時影像以做出智慧決策
- 自動調整焦距並掃描感興趣區域
- 降低光毒性並節省時間
- 實現高通量與自適應成像實驗
顯微鏡影像處理中熱門的人工智能工具
<div i='1'>一個豐富的工具生態系統支援顯微鏡中的人工智慧。研究人員已開發出多種通用與專用軟體,其中許多是開源的:</div>
Cellpose
| 開發者 | Carsen Stringer 與 Marius Pachitariu(MouseLand 研究團隊) |
| 支援平台 |
需安裝 Python(pip/conda),GUI 僅限桌面使用。 |
| 語言支援 | 英文文件;全球研究實驗室廣泛採用 |
| 收費模式 | 免費且開源,採 BSD-3-Clause 授權條款 |
概覽
Cellpose 是一款先進的深度學習分割工具,專為顯微鏡影像設計。作為通用演算法,它能準確分割多種細胞類型(細胞核、細胞質等),適用不同成像模式,無需重新訓練模型。具備人機互動功能,研究人員可微調結果,將模型適配自有資料,並應用於 2D 與 3D 影像流程。
主要功能
開箱即用,適用多種細胞類型、染色及成像模式,無需自訂訓練。
支援完整 3D 堆疊,採用「2.5D」方法重用 2D 模型處理體積資料。
手動修正分割結果,並在自訂資料上再訓練模型以提升準確度。
提供 Python API、命令列介面及圖形使用者介面,靈活支援各種工作流程。
具備去噪、去模糊及升頻功能,提升分割前的影像品質。
下載或存取
技術背景
Cellpose 由 Stringer、Wang、Michaelos 與 Pachitariu 在一項開創性研究中提出,訓練於包含超過 70,000 個分割物件 的大型多樣化資料集。此多樣性使模型能跨越細胞形狀、大小及顯微鏡設定進行泛化,大幅降低多數使用情境下的自訂訓練需求。對於 3D 資料,Cellpose 巧妙地以「2.5D」方式重用 2D 模型,避免完全 3D 標註訓練資料的需求,仍能提供體積分割。Cellpose 2.0 引入了 人機互動式再訓練,允許用戶手動修正預測並在自有影像上再訓練,以提升特定資料集的效能。
安裝與設定
使用 conda 建立 Python 環境:
conda create -n cellpose python=3.10啟動環境並安裝 Cellpose:
# For GUI support
pip install cellpose[gui]
# For minimal setup (API/CLI only)
pip install cellpose快速入門
GUI 模式
- 執行以下指令啟動 GUI:
python -m cellpose - 將影像檔案(
.tif、.png等)拖放至介面 - 選擇模型類型(例如「cyto」代表細胞質,「nuclei」代表細胞核)
- 設定預估細胞直徑,或讓 Cellpose 自動校正
- 點擊開始分割並檢視結果
Python API 模式
from cellpose import models
# Load model
model = models.Cellpose(model_type='cyto')
# Segment images
masks, flows = model.eval(images, diameter=30)微調與再訓練
- 生成遮罩後,在 GUI 中手動合併或刪除遮罩以修正分割
- 使用內建訓練功能,在修正範例上再訓練模型
- 提升模型在特定資料集上的表現
處理 3D 資料
- 載入多層 Z 軸 TIFF 或體積堆疊
- 在 GUI 或 API 中使用
--Zstack參數以 3D 模式處理 - 可選擇透過平滑或專用參數微調 3D 流以優化分割
限制與注意事項
- 模型通用性折衷:雖然通用模型適用廣泛,但極端特殊的細胞形狀或成像條件可能需重新訓練。
- 標註工作量:人機互動式訓練需手動修正,對大型資料集耗時較長。
- 安裝複雜度:GUI 安裝可能需使用命令列、conda 環境及管理 Python 相依套件,對非程式使用者不一定直覺。
- 僅限桌面:Cellpose 設計為桌面使用,無原生 Android 或 iOS 應用程式。
常見問題
不需要 — Cellpose 提供預訓練的通用模型,通常無需再訓練即可達良好效果。但若需最佳結果,特別是針對特殊或罕見資料,可利用人機互動功能進行標註與再訓練。
能 — 它透過重用 2D 模型(所謂「2.5D」)支援 3D,並可在 GUI 或 API 中處理體積堆疊。
建議使用 GPU 以加速推論與訓練,尤其是大型或 3D 資料集,但 Cellpose 也能在僅有 CPU 的機器上運行,效能較慢。
在 GUI 中可手動設定預估細胞直徑,或讓 Cellpose 自動校正。若分割效果不理想,可進行微調與再訓練。
可以 — 新版本(Cellpose 3)包含影像修復模型,具備去噪、去模糊及升頻功能,提升分割前的影像品質。
StarDist
| 開發者 | Uwe Schmidt、Martin Weigert、Coleman Broaddus 及 Gene Myers |
| 支援平台 |
|
| 語言支援 | 開源專案,文件與社群主要使用英文 |
| 收費模式 | 免費且開源。授權為 BSD-3-Clause |
概覽
StarDist 是一款用於顯微鏡影像實例分割的深度學習工具。它將每個物件(如細胞核)表示為 2D 星形凸多邊形或 3D 多面體,能精確偵測並分離密集或重疊的物件。憑藉其穩健架構,StarDist 廣泛應用於螢光顯微鏡、組織病理學及其他生物影像分析的自動細胞與細胞核分割。
主要特色
利用星形凸多邊形(2D)與多面體(3D)實現高度精確的實例分割,確保物件偵測可靠。
專為 2D 影像與 3D 體積資料設計的模型,提供完整的顯微鏡分析。
提供螢光細胞核、H&E 染色組織學及其他常見影像場景的即用模型。
在單次分割中將偵測到的物件分類為不同類別(例如不同細胞類型)。
與 ImageJ/Fiji、QuPath 及 napari 無縫整合,提供易用的 GUI 工作流程。
包含精確度、召回率、F1 分數及全景品質等完整的實例分割評估功能。
技術背景
StarDist 最初於 2018 年 MICCAI 論文中提出,其核心創新在於結合物件機率與固定射線上的徑向距離預測,能精確重建星形凸形狀。此方法能可靠分割緊密接觸且難以用傳統像素或邊界框方法分離的物件。
近期發展擴展至組織病理學影像,不僅能分割細胞核,還能對偵測物件進行多類別分類。該方法在 CoNIC(結腸細胞核識別與計數)挑戰賽中表現優異。
下載或存取
安裝與設定
安裝 TensorFlow(版本 1.x 或 2.x)作為 StarDist 的前置需求。
使用 pip 安裝 StarDist Python 套件:
pip install stardistnapari:
pip install stardist-napariQuPath: 將 .jar 檔案拖曳至 QuPath 以安裝 StarDist 擴充功能。
ImageJ/Fiji: 使用內建外掛管理器或透過外掛選單手動安裝。
執行分割
載入預訓練模型,正規化影像,並執行預測:
from stardist.models import StarDist2D
model = StarDist2D.from_pretrained('2D_versatile_fluo')
labels, details = model.predict_instances(image)在 napari 中開啟影像,選擇 StarDist 外掛,挑選預訓練或自訂模型,並直接從 GUI 執行預測。
從外掛選單使用 StarDist 外掛,透過直覺介面對影像堆疊套用模型。
安裝擴充功能後,透過 QuPath 的指令碼主控台或圖形介面執行 StarDist 偵測,適用於組織病理分析。
訓練與微調
建立每個物件皆有唯一標籤的標註影像。可使用 LabKit、QuPath 或 Fiji 等標註工具準備資料集。
使用 StarDist Python API 訓練新模型或以自訂標註資料微調既有模型。
後處理選項
- 應用非極大值抑制(NMS)以消除重複候選形狀
- 使用 StarDist OPP(物件後處理)合併非星形凸形狀的遮罩
限制與注意事項
- 星形凸假設可能無法完美模擬高度非凸或極不規則形狀
- 安裝複雜度:自訂安裝需相容的 C++ 編譯器以編譯擴充功能
- GPU 加速依賴相容的 TensorFlow、CUDA 與 cuDNN 版本
- 部分使用者反映 ImageJ 外掛因 Java 設定問題而無法正常運作
常見問題
StarDist 支援多種影像類型,包括螢光、明場及組織病理學(如 H&E 染色),得益於其靈活的預訓練模型及對不同影像模式的適應性。
可以 — StarDist 支援使用星形凸多面體進行 3D 實例分割,將 2D 功能擴展至完整的 3D 分析。
不一定。已有多款預訓練模型可直接使用,且通常效果良好。但對於專門或新穎資料,自行標註並訓練自訂模型能顯著提升準確度。
StarDist 可整合於 napari、ImageJ/Fiji 及 QuPath,讓您無需撰寫程式即可透過 GUI 執行分割,也支援直接使用 Python API 進行進階工作流程。
StarDist 內建多種常用實例分割評估指標,包括精確度、召回率、F1 分數及全景品質,協助評估分割效能。
SAM
應用資訊
| 開發者 | Meta AI 研究院(FAIR) |
| 支援裝置 |
|
| 語言與可用性 | 全球開源基礎模型;文件以英文提供 |
| 價格 | 免費 — 透過 Meta 授權於 GitHub 及 MIB 整合提供開源 |
概述
SAM(Segment Anything Model)是由 Meta 創建的強大 AI 基礎模型,能夠互動式及自動分割影像中幾乎任何物體。透過點、邊界框或粗略遮罩等提示,SAM 可生成分割遮罩,無需特定任務的重新訓練。在顯微鏡研究中,SAM 的彈性已被用於細胞分割、細胞器偵測及組織病理分析,為需要可提示、通用分割工具的研究人員提供可擴展的解決方案。
詳細介紹
SAM 最初由 Meta 在超過 10 億個遮罩及 1100 萬張影像上訓練,設計為可透過提示進行分割的基礎模型,具備新領域的「零次學習」能力。在醫學影像研究中,SAM 已被評估用於全片病理分割、腫瘤偵測及細胞核識別。然而,對於密集排列的實例(如細胞核),其表現參差不齊:即使使用大量提示(例如 20 次點擊或框選),零次學習分割在複雜顯微影像中仍可能遇到困難。
為解決此限制,出現了領域特定的調整版本:
- SAMCell — 在大型顯微鏡資料集上微調,實現跨多種細胞類型的強大零次學習分割,無需每次實驗重新訓練
- μSAM — 於超過 17,000 張手動標註的顯微鏡影像上重新訓練,以提升對小型細胞結構的準確度
主要特點
使用點、框及遮罩進行靈活互動,精確控制分割結果。
無需在新影像領域微調即可執行分割。
可透過少量樣本或提示進行顯微鏡及組織病理的再訓練。
於顯微鏡影像瀏覽器(MIB)中提供,支援 3D 及插值分割。
IDCC-SAM 可在免疫細胞化學中自動計數細胞,無需手動標註。
下載或存取
使用指南
- 開啟顯微鏡影像瀏覽器並前往 SAM 分割面板
- 設定 Python 解譯器並選擇 SAM-1 或 SAM-2 模型
- 若需 GPU 加速,請在執行環境中選擇「cuda」(建議以獲得最佳效能)
- 點提示:點擊物體以定義正向種子;使用 Shift + 點擊 擴展,Ctrl + 點擊 設定負向種子
- 3D 堆疊:使用互動式 3D 模式—點擊單張切片,Shift 滾動並在切片間插值種子
- 調整模式:根據需要替換、添加、減去遮罩,或建立新圖層
- 在 SAM-2 面板中使用 MIB 的「自動全部」選項,分割區域內所有可見物體
- 分割後檢視並視需要微調遮罩
- 使用基於提示的微調流程(如「All-in-SAM」)從稀疏用戶提示生成像素級標註
- 細胞計數可應用 IDCC-SAM,結合 SAM 的零次學習流程與後處理
- 高精度細胞分割則使用在顯微鏡細胞影像上微調的 SAMCell
限制與注意事項
- 未經領域微調,零次學習在密集或重疊結構上表現不一致
- 分割品質嚴重依賴提示設計與策略
- 強烈建議使用 GPU;CPU 推理速度非常慢
- 對超高解析度全片影像及多尺度組織結構處理較為吃力
- 微調或適配 SAM 於顯微鏡影像可能需要機器學習專業知識
常見問題
可以,透過像 SAMCell 這類專為細胞分割任務微調的顯微鏡資料集版本。
不一定。使用 IDCC-SAM,可在無需手動標註的情況下進行零次學習細胞計數。
可使用基於提示的微調流程(如「All-in-SAM」)或採用在超過 17,000 張標註顯微鏡影像上訓練的 μSAM。
雖然 CPU 可行,但強烈建議使用 GPU以獲得實用的推理速度及即時互動分割體驗。
可以,MIB 的 SAM-2 整合支援 3D 分割,並可在切片間插值種子以進行體積分析。
AxonDeepSeg
| 開發團隊 | 蒙特婁理工學院與蒙特婁大學 NeuroPoly 實驗室 |
| 支援平台 |
|
| 語言 | 英文文件;全球開源工具 |
| 價格 | 免費且開源 |
概覽
AxonDeepSeg 是一款以 AI 為核心的工具,用於自動分割顯微鏡影像中的軸突與髓鞘。透過卷積神經網路,能在多種影像模式(包括 TEM、SEM 及明視野顯微鏡)中提供精確的三類分割(軸突、髓鞘、背景)。藉由自動化形態計量測量,如軸突直徑、g 比率及髓鞘厚度,AxonDeepSeg 簡化神經科學研究中的定量分析,大幅減少手動標註時間並提升重現性。
主要功能
針對 TEM、SEM 及明視野顯微鏡模式優化的即用型模型。
精確分類顯微鏡影像中的軸突、髓鞘與背景區域。
自動計算軸突直徑、g 比率、髓鞘厚度及密度等指標。
整合 Napari GUI,支援手動微調分割遮罩以提升準確度。
無縫整合至自訂流程,適用於大規模神經組織分析。
完整測試腳本確保重現性與分割結果可靠性。
技術細節
AxonDeepSeg 由 NeuroPoly 實驗室開發,利用深度學習技術提供高精度的神經科學應用分割。提供多種顯微鏡模式的預訓練模型,確保跨影像技術的多樣性。工具整合 Napari,允許互動式修正分割遮罩,提升困難資料集的準確性。AxonDeepSeg 可計算關鍵形態計量指標,支援神經組織結構與病理的高通量研究。其基於 Python 的架構方便整合至大規模軸突與髓鞘形態分析的自訂流程中。
下載或存取
安裝與設定
請確保已安裝 Python 3.8 或更新版本,接著使用 pip 安裝 AxonDeepSeg 與 Napari:
pip install axondeepseg napari執行提供的測試腳本,確認所有元件已正確安裝並正常運作。
將 TEM、SEM 或明視野顯微鏡影像匯入 Napari 或您的 Python 環境。
選擇適合您影像模式的預訓練模型,執行分割以產生軸突與髓鞘遮罩。
自動計算軸突直徑、g 比率、密度及髓鞘厚度等形態計量,並匯出 CSV 格式結果。
使用 Napari GUI 手動調整分割遮罩,合併或刪除遮罩以提升準確度。
重要注意事項
- 對新穎或未訓練的影像模式,效能可能下降
- 複雜或具挑戰性的區域可能需手動修正
- 建議使用 GPU 加速大型資料集處理;亦支援 CPU 處理
常見問題
AxonDeepSeg 支援透射電子顯微鏡(TEM)、掃描電子顯微鏡(SEM)及明視野顯微鏡,並針對各模式提供優化的預訓練模型。
是的,AxonDeepSeg 完全免費且開源,適用於學術及商業用途。
可以,AxonDeepSeg 可自動從分割影像計算軸突直徑、g 比率、髓鞘厚度及密度等指標。
建議使用 GPU 以加速大型資料集的分割,但 CPU 也支援較小規模的分析。
可以,整合 Napari GUI 可進行互動式修正與微調分割遮罩,提升困難區域的準確度。
Ilastik
| 開發者 | 歐洲分子生物學實驗室(EMBL)Ilastik 團隊及相關學術合作夥伴 |
| 支援平台 |
|
| 語言 | 英文 |
| 價格 | 免費且開源 |
概覽
Ilastik 是一款強大的 AI 驅動工具,用於互動式影像分割、分類及顯微影像資料分析。透過隨機森林分類器等機器學習技術,協助研究人員進行像素分割、物件分類、細胞追蹤及密度計數,適用於 2D 與 3D 資料集。其直覺式介面與即時回饋,使非程式設計背景的科學家也能輕鬆使用,廣泛應用於細胞生物學、神經科學及生醫影像領域。
主要功能
在標註代表區域時提供即時回饋,快速獲得分割結果。
根據形態與強度特徵對分割結構進行分類。
追蹤 2D 與 3D 時間序列顯微影像中的細胞移動與分裂。
在無需明確分割個別物件的情況下,量化擁擠區域的數量。
針對複雜 3D 體積資料提供半自動分割與直覺互動。
使用無頭命令列模式自動處理多張影像。
下載
入門指南
從官方網站下載適用於您作業系統的 Ilastik。套件包含所有必要的 Python 依賴,請依照平台指示完成安裝。
開啟 Ilastik 並選擇分析工作流程:像素分類、物件分類、追蹤或密度計數。載入您的影像資料集,支援多通道、3D 或時間序列影像。
在影像中標註少量代表性像素或物件。Ilastik 的隨機森林分類器會從標註中學習,自動預測整個資料集的標籤。
將訓練好的模型應用於整個資料集的分割或分類。匯出標記影像、機率圖或量化表格,以供後續分析與視覺化使用。
利用 Ilastik 的無頭模式,自動處理多張影像,適合大規模分析流程。
限制與注意事項
- 互動式標註對於非常大型資料集可能耗時
- 準確度依賴使用者標註的品質與代表性
- 記憶體需求— 超高解析度或多 GB 資料集可能需要大量 RAM
- 複雜資料— 隨機森林分類器在高度變異或複雜影像資料上,表現可能不及深度神經網路
常見問題
能,Ilastik 完全支援 3D 體積與時間序列實驗,用於分割、追蹤及多時間點的量化分析。
是的,Ilastik 完全免費且開源,所有使用者皆無需授權限制。
不需要,Ilastik 提供直覺的圖形介面與即時回饋,讓無程式背景的研究人員也能輕鬆使用。進階使用者亦可利用命令列批次處理功能。
能,專用的追蹤工作流程可分析 2D 與 3D 時間序列資料中的細胞移動與分裂,並自動追蹤細胞系譜。
分割結果可匯出為標記影像、機率圖或量化表格,方便與後續分析工具及視覺化軟體整合。
這些工具涵蓋初學者到專家等級,許多為免費且開源,有助於研究社群建立可重現且共享的人工智能工作流程。
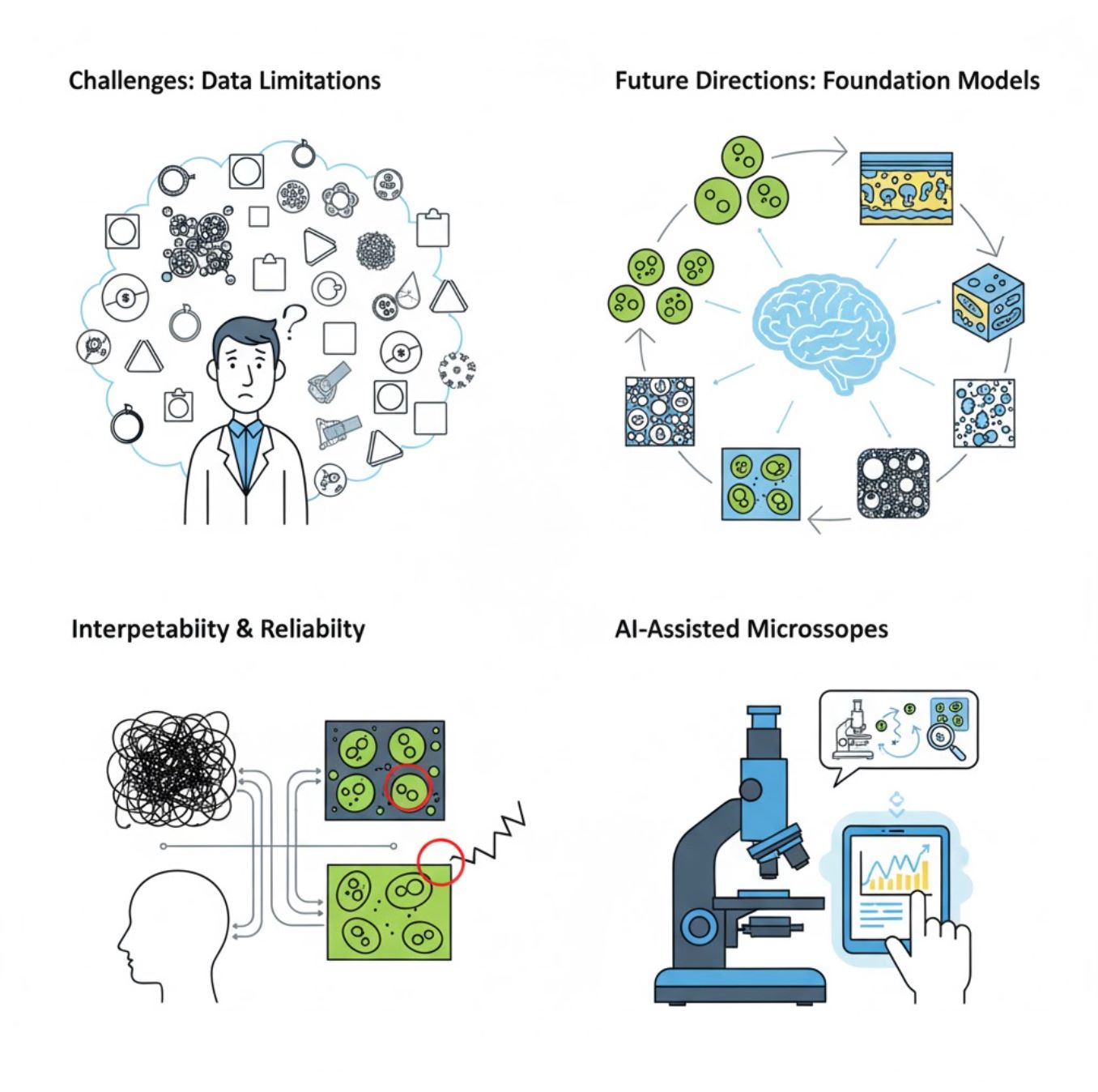
挑戰與未來方向
當前挑戰
新興趨勢
視覺基礎模型
次世代人工智能系統有望減少對特定任務訓練的需求。
- 如SAM與基於CLIP的系統
- 一套人工智能可處理多項顯微鏡任務
- 部署與適應更快速
人工智能輔助顯微鏡
完全自主且智慧的顯微鏡系統正逐漸成真。
- 透過大型語言模型自然語言控制
- 全自動反饋迴路
- 普及先進顯微鏡技術的使用
主要結論
- 人工智能正快速改變顯微鏡影像處理,提升準確度與自動化
- 深度學習在複雜且多變的顯微影像中勝過傳統機器學習
- CNN自動從原始像素學習階層特徵,實現穩健分析
- 主要應用包括分割、分類、追蹤、降噪與自動擷取
- 成功依賴高品質資料與專家嚴謹驗證
- 視覺基礎模型與人工智能輔助顯微鏡代表未來趨勢
隨著持續進步與社群努力(開源工具、共享資料集),人工智能將日益成為顯微鏡的「眼睛」核心,幫助科學家看見未曾見過的世界。







No comments yet. Be the first to comment!